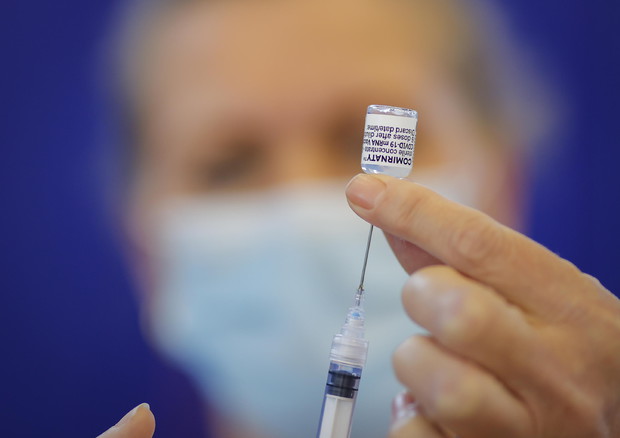
Vaccinare il maggior numero di persone possibile per frenare definitivamente la diffusione del virus SarsCoV2. E' per questo che - dopo anziani, fragili e adulti - è iniziata la corsa per la messa a punto di 'vaccini baby', adatti all'immunizzazione dei giovanissimi a partire dai 6 mesi di età.
Le aziende farmaceutiche hanno già avviato gli studi e prevedono tempi relativamente brevi: Pfizer conta infatti di arrivare ad un via libera degli enti regolatori entro l'inizio del 2022 e anche Moderna ha avviato i test, mentre il presidente della Società italiana di pediatria Alberto Villani sottolinea come questa rappresenti una "importante opportunità".
"Prevediamo che i risultati della sperimentazione del vaccino anti-Covid Pfizer-BioNTech nei bambini tra 6 mesi e 11 anni saranno disponibili nella seconda metà del 2021: se la sicurezza e immunogenicità saranno confermate, speriamo di ricevere l'autorizzazione per la vaccinazione di questi bambini più piccoli entro l'inizio del 2022", ha reso noto Pfizer all'ANSA. Dallo scorso marzo, l'azienda ha infatti inoculato il proprio vaccino ai primi bambini sani in uno studio globale di fase 1/2/3 per valutarne ulteriormente sicurezza, tollerabilità e immunogenicità. E' prevista l'inoculazione di due dosi a circa 21 giorni di distanza in tre gruppi di età: bambini dai 5 agli 11 anni, dai 2 ai 5 anni e dai 6 mesi ai 2 anni.
Anche l'azienda Moderna guarda al 'baby vaccino', ed ha arruolato 3000 ragazzi tra 12 e 17 anni di età per i test avviati in Usa. Un altro studio di fase 2-3 è stato avviato anche sui bambini più piccoli, tra 6 mesi e 11 anni, e si punta ad arruolare complessivamente 6.750 bambini sani in Usa e Canada a cui verranno date due dosi di vaccino a distanza di 28 giorni.
Il fatto che in Italia "resti il dato che su oltre 120mila decessi complessivi da Covid-19 ci siano stati meno di 30 decessi in età evolutiva - spiega Villani - non fa sì che si ritenga che non sia fondamentale fare il vaccino anche ai bambini". Infatti, "pur essendo quella delle complicanze e dei decessi una evenienza estremamente rara nei bambini, almeno nel nostro Paese, è pur vero che anche in Italia un soggetto pediatrico su 1000 arriva a sviluppare la Sindrome infiammatoria multiorgano che è una patologia molto grave".